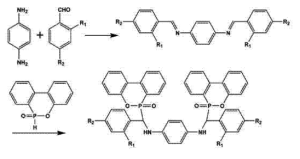
8-羥基喹啉的電導率特性及其在不同條件下的變化規律
發表時間:2025-12-168-羥基喹啉是一種弱電解質類有機化合物,分子含羥基(-OH) 和吡啶環氮原子兩個可解離位點,其電導率特性源于分子的微弱解離行為,且受濃度、溶劑極性、pH值、溫度等因素調控,在電化學檢測、金屬離子配位傳感等領域具有重要應用價值。
一、電導率基礎特性
1.純品與溶液的電導率表現
純固態/熔融態8-羥基喹啉:常溫下為結晶粉末,分子間通過氫鍵、π-π堆積形成致密結構,無自由移動的離子,電導率極低(<10⁻⁸S/m),屬于絕緣體;熔融態時分子排列松散,但解離程度仍極低,電導率僅輕微提升(約10⁻⁷~10⁻⁶S/m)。
8-羥基喹啉溶液:溶解于極性溶劑后,分子發生微弱解離,產生少量可移動離子,電導率顯著升高,具體解離平衡如下:
羥基解離:C9H6NOH⇄C9H6NO-+H+,pK a1≈9.9;
吡啶環氮原子質子化:C9H6NOH+H+⇄C9H7NOH+,pK a2≈4.9。
以水溶液為例:
極低濃度(<0.001mol/L)時,解離度低,電導率約5~10μS/cm;
濃度升高至 0.01~0.1mol/L 時,離子濃度增加,電導率升至20~50μS/cm;
濃度超過臨界膠束濃度(CMC,約0.05mol/L)后,分子形成膠束,解離受到抑制,電導率增長趨于平緩。
2.電導率的本質與應用意義
8-羥基喹啉溶液的電導率直接反映解離產生的離子濃度,其電導率變化可用于判斷分子的解離平衡移動、膠束形成過程,以及與金屬離子的配位反應(配位后離子形態改變,電導率會出現特征性變化),例如,在金屬離子檢測中,8-羥基喹啉與、等形成配位化合物,導致溶液電導率下降,可通過電導率變化實現金屬離子的定性與定量分析。
二、影響8-羥基喹啉電導率的關鍵因素及變化規律
1.濃度:核心影響因素,呈“上升-飽和”趨勢
8-羥基喹啉溶液的電導率與濃度的關系遵循弱電解質的變化規律:
濃度低于CMC時:電導率隨濃度升高近似線性增長。原因是濃度升高使解離的離子總數增加,且分子未形成膠束,解離平衡不受顯著抑制。
濃度高于CMC時:電導率增長速率顯著放緩并趨于穩定。此時多余的分子在溶液中聚集形成膠束,膠束內部的分子難以解離,離子濃度不再隨濃度升高而大幅增加。
對比:強電解質(如NaCl)的電導率隨濃度升高先升后降(因離子間相互作用增強),而8-羥基喹啉作為弱電解質,無電導率下降階段,僅表現為增長飽和。
2.溶劑極性:決定解離程度,極性越強電導率越高
溶劑的極性通過影響分子的解離能和離子的溶劑化作用,調控8-羥基喹啉的電導率,規律如下:
強極性溶劑(水、甲醇、乙醇):溶劑分子可與8-羥基喹啉的解離離子形成穩定溶劑化層,降低離子間的締合作用,促進解離,電導率較高,例如:0.01mol/L 8-羥基喹啉的水溶液電導率>甲醇溶液>乙醇溶液。
弱極性/非極性溶劑(丙酮、苯、石油醚):難以溶劑化離子,分子解離程度極低,電導率僅為1~5μS/cm,接近溶劑本身的電導率。
混合溶劑:可通過調整極性比例精準調控電導率,例如,在乙醇-水混合溶劑中,隨著水的比例增加,溶劑極性增強,電導率呈線性上升。
3. pH值:調控解離平衡,呈“U型”變化規律
8-羥基喹啉的兩個解離位點對pH值敏感,溶液pH值通過改變分子的解離形態,影響電導率,變化規律呈U 型曲線:
強酸性條件(pH<3):吡啶環氮原子被質子化,生成陽離子,解離平衡向右移動,離子濃度升高,電導率顯著上升。
中性條件(pH 6~8):分子主要以中性形態存在,解離程度很低,離子濃度少,電導率處于至低值區間。
強堿性條件(pH>11):羥基發生解離,生成陰離子,解離平衡向右移動,離子濃度增加,電導率再次上升。
這一特性是8-羥基喹啉作為pH響應型電化學材料的核心依據。
4.溫度:提升離子遷移速率,電導率隨溫度升高而上升
溫度對電導率的影響體現在兩個方面:
溫度升高促進分子解離,使溶液中離子濃度增加;
溫度升高提升離子的遷移速率(降低溶劑黏度,減少離子運動阻力)。
因此,8-羥基喹啉溶液的電導率與溫度呈正相關:每升高10℃,電導率約提升10%~15%。例如,0.01mol/L水溶液在25℃時電導率為30μS/cm,35℃時可達33~35μS/cm。
注意:溫度過高(>60℃)會導致8-羥基喹啉分子分解,反而使電導率下降。
5.金屬離子:發生配位反應,電導率顯著下降
8-羥基喹啉是典型的金屬離子螯合劑,可與、、等過渡金屬離子形成電中性的配位化合物,導致溶液電導率下降:
配位反應式(以為例):;
變化規律:隨著金屬離子濃度增加,電導率持續下降,直至8-羥基喹啉完全配位,電導率降至穩定低值(接近溶劑電導率)。
這一現象可用于金屬離子的電化學檢測,通過電導率突變判斷配位反應的終點。
三、電導率測定的注意事項
溶劑背景校正:測定前需先測定純溶劑的電導率,扣除背景值,避免溶劑雜質對結果的干擾。
恒溫條件控制:溫度對電導率影響顯著,需在恒溫(如25±0.1℃)環境下測定,確保數據重復性。
避免濃度過高:濃度超過CMC后電導率變化無顯著意義,多數實驗選擇0.001~0.05mol/L 的濃度區間。
本文來源于黃驊市信諾立興精細化工股份有限公司官網 http://m.narui-group.com/

 ronnie@sinocoalchem.com
ronnie@sinocoalchem.com 15733787306
15733787306